挥之不去与无忧无虑:一篇关于痤疮发病机制的通俗综述
挥之不去与无忧无虑:一篇关于痤疮发病机制的通俗综述
Rubbish编辑部Hongzhang Wang1, Casey Wellington2 and Dedaowu3、
阅读 PDF 全文Abstract
摘要
痤疮是一种常见的毛囊皮脂腺慢性炎症性皮肤病,尤其在青少年及年轻成人中高发,影响患者的外貌和心理健康。本文旨在以通俗易懂的语言,讲解机制的研究进展,包括皮脂过度分泌、毛囊导管角化异常、微生物群落失衡及免疫炎症反应等方面。通过形象化的比喻和简明的科学解释,帮助非专业读者理解痤疮的成因及其背后的生物学基础。本文不涉及药物治疗内容,适用于科普教育和科研入门阅读。
Keywords: Acne vulgaris; Pathogenesis; Sebaceous gland; Inflammation; Microbiome
关键词: 痤疮;发病机制;皮脂腺;炎症;微生物
1. Introduction
1. 引言
痤疮,俗称“青春痘”,是皮肤科最常见的疾病之一。尽管其发病率高,但公众对其成因的了解往往停留在“上火”或“清洁不当”等表面认识。事实上,痤疮的发生是一个多因素共同作用的复杂过程,涉及内分泌、免疫、微生物和遗传等多个方面。本文以通俗的语言和形象的比喻,系统梳理痤疮发病机制的四大核心环节,帮助读者建立科学的认知框架,消除误解,提升健康素养。
2. The pathogenesis of acne vulgaris
2. 痤疮的发病机制
时至今日,学界对痤疮的发病机制认识仍不全面,其影响因素多样,目前认为主要与雄激素诱导下皮脂的过度分泌、毛囊皮脂腺导管角化异常的出现以及微生物增殖和免疫应答有关,各因素之间也存在一定相互作用关系,不断加重炎症从而产生痤疮¹²。
2.1 Excessive sebum production
2.1 皮脂分泌过度
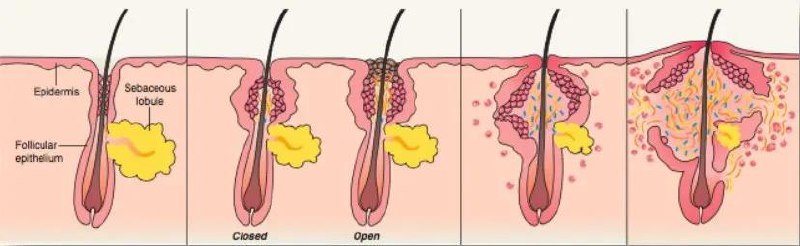
皮脂腺是皮肤里的微型腺体,遍布全身(手掌脚底除外),在面部、前胸和后背最密集。它分泌皮脂排到皮肤表面,形成保护膜防止干燥。但当雄激素刺激它过度产油,加上毛囊导管堵塞,皮脂排不出去,就成了痤疮丙酸杆菌的“食物”而且其自身也会发生变化导致炎症³,触发炎症反应,痤疮就此发生。

皮脂腺就像皮肤里的“微型油厂”,正常情况下生产适量油脂来保护皮肤。但在痤疮患者身上,这家工厂被强行“超产”了。
雄激素是其背后最大的推手。进入青春期后,体内的雄激素水平上升,睾酮在皮肤内被转化为一种叫“双氢睾酮”物质,它直接刺激皮脂腺细胞,命令它们拼命产油。这就是为什么青春期最容易长痘⁴。
但问题来了:很多长痘的女性查血,雄激素水平并不高,怎么回事?研究发现,她们的皮脂腺对雄激素“太敏感”——工厂里的“接收器”(雄激素受体)太多或太灵敏,一点点激素就能引发过度反应。
尽管雄激素常被视为男性激素,但其在女性痤疮发病中同样起核心作用。女性体内雄激素主要来源于肾上腺和卵巢,可通过影响皮脂腺功能参与痤疮发生。临床上,部分女性痤疮患者尤其是伴有月经前加重或多囊卵巢综合征时,常存在雄激素水平异常或受体敏感性增高。
胰岛素样生长因子-1(IGF-1)是另一个“加油工”。吃甜食、喝牛奶会让体内IGF-1水平升高,它通过一条叫“PI3K/Akt/mTORC1”的信号通路,不仅直接刺激皮脂腺,还能增强雄激素的效果。这就解释了为什么高糖饮食会加重痘痘⁵。
神经信号也能参与。压力大的时候,皮肤神经末梢会释放一种叫“P物质”的东西,它也能刺激皮脂腺产油。所以“一紧张就长痘”不是心理作用,有生理基础。
2.2 Abnormal follicular epithelial keratinization
2.2 毛囊皮脂腺导管角化异常
皮脂产出来了,得有个出口排出去——这个出口就是毛囊导管。而在大多数痤疮患者身上,导管内壁的细胞(角质形成细胞)过度增生,还黏在一起不掉落,导致管口越来越窄,最终堵死。
一部分问题出在油脂成分变了。正常皮脂里有一种叫“亚油酸”的成分,它能维持导管细胞正常脱落。痤疮患者的皮脂里亚油酸太少,细胞就掉不下来。同时,皮脂里的“角鲨烯”被氧化成“角鲨烯过氧化物”,这种东西会直接刺激导管内壁的细胞增生,让堵塞更严重。
还有一种叫“IL-1α”的炎症因子也在搞破坏。它在粉刺里含量很高,实验证明只要把它加到毛囊培养液里,就会诱导导管角化。这个发现很重要——说明炎症在粉刺形成阶段就已经参与了,不是后期才来。
2.3 Re-evaluation of the role of microbial dysbiosis and Cutibacterium acnes
2.3 微生物群落失衡与痤疮丙酸杆菌的作用再认识
毛囊里本来就住着细菌,主要是“痤疮丙酸杆菌”。其大量繁殖与痤疮形成密切相关。
但是痤疮患者为什么发病呢?关键是菌株不同。研究发现,健康人的毛囊里和痤疮患者的毛囊里都有这种菌,但种类不同。致病性强的菌株(比如IA型)在患者身上更多,它们会释放更多刺激炎症的物质;而健康人身上多是相对致病性差菌株(II型、III型),甚至能帮着抗炎。所以,问题不光是细菌过多,更是菌群失衡了。
其通过以下方式致病(包括但不限于):
- 激活免疫警报:细菌的细胞壁成分能被毛囊周围的免疫细胞识别,通过一种叫“Toll样受体2”的开关,启动炎症反应,释放TNF-α、IL-1等信号。
- 产生生物膜:细菌会分泌一层黏糊糊的东西把自己包裹起来,形成生物膜。这层膜会让药物和免疫细胞都难以进入,导致炎症持续不退。
2.4 Inflammation and immune response
2.4 炎症与免疫应答
这是一个关键观念更新:炎症不是毛囊被撑破后才发生,而是从长痘一开始就存在。
在肉眼还看不见粉刺的时候,毛囊周围已经有免疫细胞( 细胞)聚集,血管也做好了迎接炎症细胞的准备。也就是说,炎症是痤疮的“启动事件”,而不是“最终结果”。
先天免疫系统率先反应。前面提到的Toll样受体2属于先天免疫,它被激活后,会通过一系列信号,最终调动“炎症小体NLRP3”。这个炎症小体像一把剪刀,剪出成熟的IL-1β——后者是放大炎症的关键分子。
适应性免疫随后加入。如果炎症持续,身体就会启动更精确的免疫。痤疮患者体内出现了针对痤疮丙酸杆菌的“Th1”和“Th17”细胞,它们分泌IFN-γ和IL-17,这些信号会吸引更多中性粒细胞过来,导致组织损伤。这也解释了为什么有些人痘痘此起彼伏、难以治愈——免疫系统已经耿耿于怀了。
持续不断的炎症不仅让皮肤发红、化脓,还会释放一些降解组织的酶,最终导致瘢痕的形成。
3. Conclusion
3. 结语
痤疮的发病机制,说到底是一场发生在毛囊里的“多米诺骨牌”:雄激素推倒了第一块,皮脂分泌随之失控;角化异常紧随其后,堵住了出口;微生物趋势而起,免疫系统闻风而动——环环相扣,层层递进。
写这篇综述时,我们试图用最朴素的语言,把这套复杂的机制讲清楚。不是为了简化科学,而是为了让更多人知道:长痘这件事,既不“脏”,也不“上火”,它是一套精密的生物学剧本,写在基因里,演在皮肤上。
愿每一位正在解码这场“皮肤风暴”的科研者,都能在数据的汪洋中找到属于自己的那块多米诺骨牌;愿你们的实验一帆风顺,细胞听话,审稿人温柔。也愿每一个被痘痘困扰的人,在了解它之后,能少一分焦虑,多一分从容。
痤疮或许挥之不去,但愿你我都能在科研与生活中,保持一份无忧无虑。
Funding
自燃科学基金(10086)
国际起痘协会科学基金(10010)
Declaration
本文为科普性质,旨在以通俗易懂的方式介绍痤疮的发病机制,不涉及任何药物推荐或治疗方案。所有作者均声明无任何利益冲突。本文内容基于公开的科学研究文献,仅供读者参考学习,不作为临床诊断或治疗依据。如有皮肤问题,请咨询专业医师。
References
- 潘清丽,邵蕾,陈丽洁,王建琴.痤疮发病机制的研究进展.皮肤性病诊疗学杂志.2018;25(6):377-380.
- 孙欣荣,刘志宏,黄爱文,杨海跃,宋洪涛.痤疮发病机制及其药物治疗的研究进展.中国药房.2017;28(20):2868-2871.
- Makrantonaki E, Ganceviciene R, Zouboulis C. An update on the role of the sebaceous gland in the pathogenesis of acne. Derm-Endocrinol. 2011;3(1):41-49. doi:10.4161/derm.3.1.13900
- 黄善聪,陈力.血清性激素水平对痤疮发病的影响及治疗.辽宁中医药大学学报. 2013;15(11):169-171. doi:10.13194/j.issn.1673-842x.2013.11.109
- Jahns AC, Eilers H, Ganceviciene R, Alexeyev OA. Propionibacterium species and follicular keratinocyte activation in acneic and normal skin. Br J Dermatol. 2015;172(4):981-987. doi:10.1111/bjd.13436
- 靳培英.痤疮的分型论治.中华皮肤科杂志. 2002;(1):66-68.
- Yu Y, Champer J, Agak GW, Kao S, Modlin RL, Kim J. Different propionibacterium acnes phylotypes induce distinct immune responses and express unique surface and secreted proteomes. J Invest Dermatol. 2016;136(11):2221-2228. doi:10.1016/j.jid.2016.06.615
- Selway JL, Kurczab T, Kealey T, Langlands K. Toll-like receptor 2 activation and comedogenesis: implications for the pathogenesis of acne. BMC Dermatol. 2013;13:10. doi:10.1186/1471-5945-13-10
- Huang C, Zhuo F, Han B, et al. The updates and implications of cutaneous microbiota in acne. Cell Biosci. 2023;13(1):113. doi:10.1186/s13578-023-01072-w
- Zouboulis CC, Jourdan E, Picardo M. Acne is an inflammatory disease and alterations of sebum composition initiate acne lesions. J Eur Acad Dermatol Venereol: JEADV. 2014;28(5):527-532. doi:10.1111/jdv.12298
- Harvey A, Huynh TT. Inflammation and acne: putting the pieces together. J Drugs Dermatol: JDD. 2014;13(4):459-463.
- 张鲁,隋长霖,魏艳杰,张佩莲.痤疮内在因素发病机制的研究进展.皮肤科学通报. 2024;41(6):690-694.
- Contassot E, French LE. New insights into acne pathogenesis: propionibacterium acnes activates the inflammasome. J Invest Dermatol. 2014;134(2):310-313. doi:10.1038/jid.2013.505
本博客所有文章除特别声明外,均采用 CC BY-NC-SA 4.0 许可协议。转载请注明来自 Rubbish!